新生儿呼吸系统疾病
在美国,新生儿呼吸窘迫症候群(RDS)每年影响大约4万名 婴儿。虽然死亡率在过去几十年大幅下降,但仍有许多婴儿死亡或患有与治疗该症候群有关的慢性疾病(如氧气和正压)。
新生儿呼吸窘迫症候群(RDS)是一种早产儿疾病。发病率随胎龄的减少而增加,在28周以内的新生儿中超过80%发生。 RDS病理生理学的主要因素包括表面活性剂缺乏、肺泡单位和毛细血管发育不全、肺泡表面积减少、肺顺应性降低、气体交换不良和动脉导管的存在。
病理生理学

概述与新生儿呼吸窘迫症候群(RDS)相关的病理生理事件。表面张力素的下降使得肺泡表面张力增加,导致肺泡变得不稳定和塌陷,肺扩张不全和呼吸功(WOB)增加。
同时,增加的表面张力也会增加积液,从毛细血管进入肺泡。
总之,这些因素损害了氧气(O2)交换,并导致严重的低氧血症。严重低氧血症和酸中毒增加肺血管阻力(PVR)。
随着肺动脉压升高,肺动脉右向左分流增加,低氧血症加重。
低氧血症和酸中毒影响表面张力素的进一步生产。
临床表现
在出生后不久就会出现呼吸窘迫的最初症状。通常首先出现呼吸急促,接下来可能会观察到严重的凹陷、反常呼吸和可听到的咕噜声,也可以看到鼻部扩张。胸部听诊常可发现细微的吸气爆裂音(crackles)。发绀可能存在,也可能不存在,如果观察到中央发绀,婴儿很可能有严重的低氧血症。某些其他情况,如全身低血压、体温过低和体温过低灌注,可以模拟呼吸窘迫症候群(RDS)的这方面。
呼吸窘迫症候群(RDS)的明确诊断通常是胸部x光片。典型的呼吸窘迫症候群(RDS)表现为弥漫、模 糊、毛玻璃样或网状颗粒状密度,并伴有肺容量低的支气管充气图。网状颗粒状结构(reticulogranular pattern)是由呼吸细支气管通气和广泛的肺泡塌陷所引起的。支气管充气图表现为充气,深色,主支气管塌陷或质变的肺组织所包围。

治疗
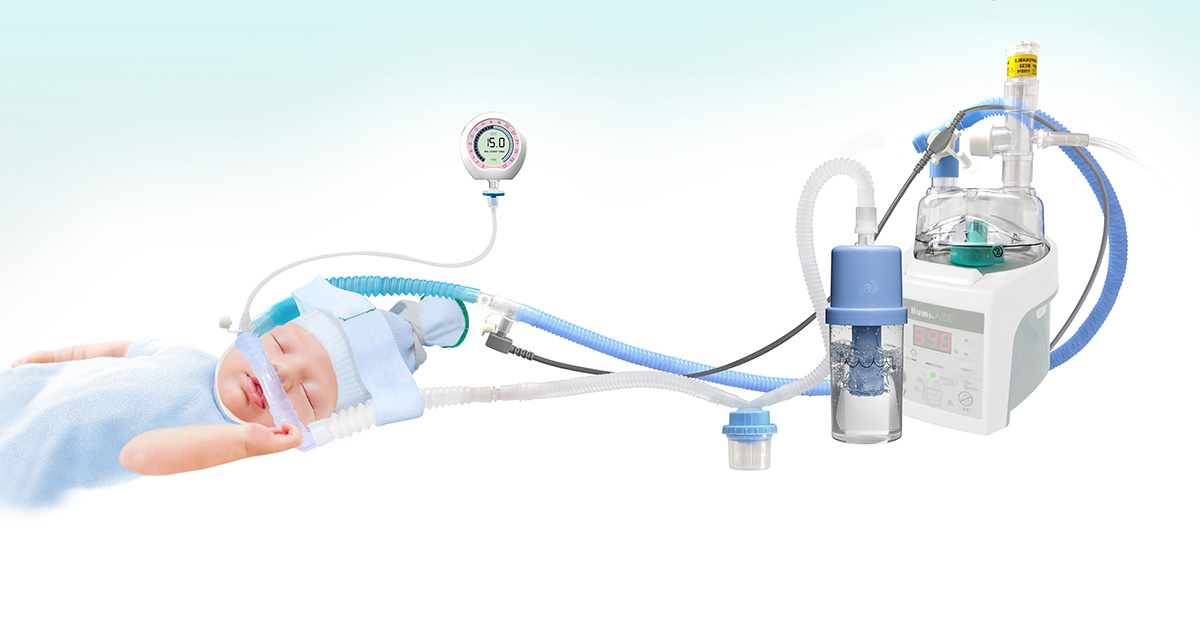
连续气道正压(CPAP)、表面张力素替代治疗和机械通气与常规或高频通气(HFV),是呼吸窘迫症候群(RDS)常用的措施,高流量鼻插管(HFNC),鼻间歇强制通气(NIMV),则当婴儿的情况严重(呼吸功增加高, FiO₂>0.4,和严重呼吸暂停),需要进行连续气道正压(CPAP)试验(4至6cm H₂O)。
由于气管内导管(ETTs)的危害,鼻管(nasal prong)或面罩(nasal mask)是首选。如果婴儿的临床状况迅速恶化,则需要更积极的治疗方法。如果连续气道正压(CPAP)对气体交换没有改善,或者患者的频繁呼吸暂停对刺激没有反应,则应启动吐气末正压(PEEP)机械通气。
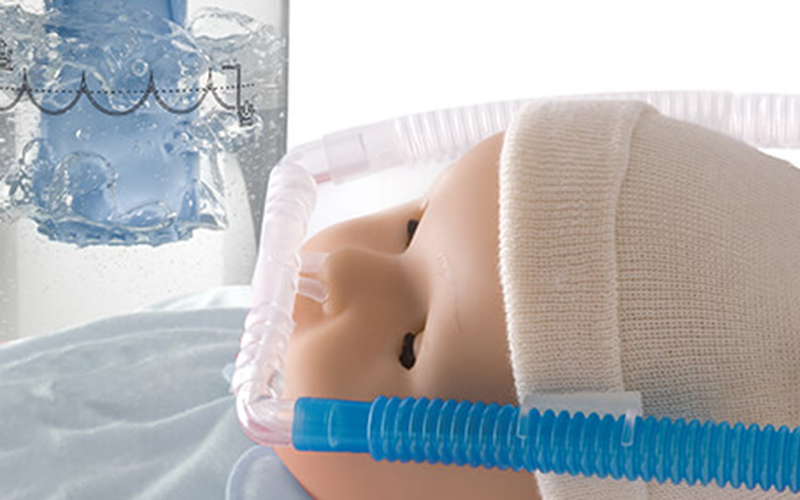
Bubble CPAP
水下气泡CPAP (B-CPAP)和呼吸机源CPAP (V-CPAP)是两种最常用的CPAP模式,它们使用不同的压力源。在V-CPAP中,调节阀门中的可变电阻以提供空气流动的阻力。在B-CPAP中,正压是通过吐气管浸入到所需深度的水柱中而不是使用可变电阻来实现的。
根据研究Iran J Pediatr. 2011 Jun; 21(2): 151–158,结果表明,B-CPAP在治疗早产儿呼吸窘迫症候群(RDS)方面优于V-CPAP,其并发症少,住院时间短,费用低。与V-CPAP相比,B-CPAP的简单性和低成本使其在资源贫乏的环境中成为一个有吸引力的选择。